|
aminokwas
Związki organiczne, pochodne węglowodorów, zawierające co najmniej jedną grupę aminową
(-NH2) i jedną grupę karboksylową (-COOH). Są to więc kwasy karboksylowe (alifatyczne lub aromatyczne), zawierające w
cząsteczce oprócz grupy karboksylowej -COOH, grupę aminową -NH2.

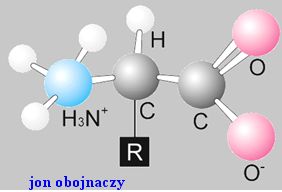 Konsekwencją obecności grupy karboksylowej i grupy aminowej jest możliwość oddziaływań, czy wręcz reakcji, zachodzących w obrębie jednej cząsteczki posiadającej
kwasową grupę karboksylową i zasadową grupę aminową. Możliwe są oczywiście także oddziaływania międzycząsteczkowe tych grup, pochodzących z różnych cząsteczek.
Konsekwencją obecności grupy karboksylowej i grupy aminowej jest możliwość oddziaływań, czy wręcz reakcji, zachodzących w obrębie jednej cząsteczki posiadającej
kwasową grupę karboksylową i zasadową grupę aminową. Możliwe są oczywiście także oddziaływania międzycząsteczkowe tych grup, pochodzących z różnych cząsteczek.
Klasyfikacja aminokwasów
Aminokwasy alifatyczne
Zawierają w cząsteczkach grupy funkcyjne aminowe i karboksylowe związane z nasyconymi, tetraedrycznymi atomami węgla. Ze względu na położenie
grupy aminowej w stosunku do grupy karboksylowej w cząsteczce dzieli się je na α, β, γ, δ, ε… - aminokwasy.
Przykłady:
-
H2N-CH2-COOH – α–aminokwas (gr -COOH i –NH2 są połączone z tym samym At. C)
-
H2N-CH2-CH2-COOH – β–aminokwas
-
H2N-CH2-CH2-CH2-COOH – γ–aminokwas
Aminokwasy aromatyczne
Obie grupy funkcyjne związane są z atomami węgla pierścieni aromatycznych.
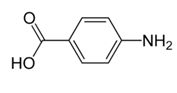
kwas p-aminobenzoesowy
Rozpuszczalność i temperatura topnienia
Jonowa budowa aminokwasów wpływa na ich rozpuszczalności. Większość aminokwasów białkowych jest rozpuszczalna w
wodzie, a prawie wszystkie, za wyjątkiem proliny, są trudno lub w ogóle nierozpuszczalne w rozpuszczalnikach organicznych, nawet
polarnych, takich jak alkohole czy ketony. Z kolei aminokwasy aromatyczne, kwasowe a także cysteina trudno rozpuszczają się w
wodzie, tzn. ich rozpuszczalność w temperaturze pokojowej nie przekracza 1g w 100cm3. Do najtrudniej rozpuszczalnych należą cysteina, tyrozyna,
histydyna, kwas asparaginowy oraz kwas glutaminowy. Najłatwiej natomiast w wodzie rozpuszczają się hydroksyprolina i glicyna.
Aminokwasy białkowe wykazują dobrą rozpuszczalność w wodnych i alkoholowych roztworach kwasów nieorganicznych, w amoniaku i w
wodnych roztworach zasad, takich jak roztwór węglanu sodu lub potasu.
Wszystkie aminokwasy są substancjami krystalicznymi, które wykazują wysokie temperatury topnienia. Najczęściej temperatura rozkładu aminokwasów
białkowych przekracza 200oC, a w niektórych przypadkach nawet 300oC. Wysokie temperatury topnienia aminokwasów wynikają z ich jonowej budowy.
Znaczenie aminokwasów
Aminokwasy są związkami biologicznie ważnymi jako materiał budulcowy wszystkich białek, w których połączone są wiązaniami peptydowymi. Niektóre
aminokwasy stanowią produkty wyjściowe do biosyntezy ważnych hormonów np. z tyrozyny powstaje tyroksyna i adrenalina.
Rośliny mogą syntetyzować wszystkie aminokwasy, zwierzęta są zdolne do syntezy tylko niektórych (aminokwasy endogenne), zaś pozostałe (aminokwasy egzogenne)
muszą pobierać z pokarmem.
Inne hasła zawierające informacje o "aminokwas":
Miozyna
grubych i
elastyny
. Miozyna była jednym z pierwszych białek o poznanej sekwencji
aminokwasów
, sekwencji
mRNA
, oraz oznaczonej konformacji przestrzennej łańcucha polipeptydowego. Podobne białkowe
włókna
...
Związek organiczny
za nieorganiczne jeszcze przed działalnością Wöhlera, takie jak
węglany
. Klasyfikacja
Glicyna
stanowi najprostszy aminokwas białkowy a zarazem przykład związku wielofunkcyjnegoIstnieje kilka możliwości dokonania podziału związków ...
Kwashiorkor
(
białko
,
witaminy
,
pierwiastki śladowe
) pożywienia. Niedobory żywieniowe zaburzają
syntezę
enzymów
, niedostateczna
podaż
aminokwasów
prowadzi do zmian funkcji, a potem również struktury
narządów
wewnętrznych, wtórnie ...
Fosforylacja oksydacyjna
siarki. Każdy z atomów żelaza wchodzących w skład centrów jest koordynowany przez
aminokwas
, zwykle grupę -SH
cysteiny
. Jony metalu, tworzącego kofaktor, ulegają redukcji podczas ...
Dorothy Crowfoot Hodgkin
prowadziła w Cavendish Laboratory w Cambridge badania krystalograficzne nad
sterolami
,
peptydami
i
aminokwasami
. Następnie ponownie pracowała w Uniwersytecie w Oxfordzie. W 1937 obroniła doktorat ...
Historia nauki
Śniadecki
sformułował koncepcję obiegu materii w przyrodzie. W
1805
pierwszy raz wyizolowano
aminokwas
asparaginę
.
Aleksander von Humboldt
, niemiecki uczony i podróżnik, badał geologię i ...
Plemnik
ssaków. Zasadowe
keratynopodobne
białka
histonowe
plemników
buhaja
składają się z 47 reszt
aminokwasowych
z
alaniną
jako N-końcowym oraz
glutaminą
jako C-końcowym aminokwasem.Funkcja białek zasadowych:udział ...
Wiązanie peptydowe
Wiązanie peptydowe - umowna nazwa
wiązania amidowego
występującego między aminokwasami peptydów i białek. Wiązanie peptydowe łączy
grupę α-aminową
jednego aminokwasu z ...
Dwupeptydy
Dwupeptydy –
organiczne
związki chemiczne
zbudowane z dwóch reszt
aminokwasowych
połączonych
wiązaniem peptydowym
. W organizmach żywych powstają na drodze biosyntezy, są ...
Wiązanie wodorowe
których przyłączone są różne podstawniki, charakterystyczne dla 20 różnych istniejących w przyrodzie
aminokwasów
biogennych. Grupy
aminowa
i
karbonylowa
tworzą wewnątrzcząsteczkowe wiązanie wodorowe N-H...O=C, które ...
Inne lekcje zawierające informacje o "aminokwas":
102. Nieorganiczne i organiczne składniki komórki cz.2 (plansza 10)
...
102. Nieorganiczne i organiczne składniki komórki cz.2 (plansza 15)
...
Białka (plansza 3)
...
|