Wiele zjawisk dotyczących kinetyki chemicznej można wytłumaczyć na gruncie
teorii zderzeń.
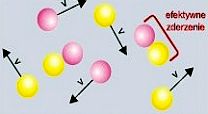
Podczas reakcji substancji A z substancją B konieczne jest, aby cząstki A (mogą
to być cząsteczki, jony lub atomy) zderzały się
z cząstkami B.
W zderzeniu następuje przegrupowanie atomów
i elektronów, powodujące przemianę wiązań chemicznych, czyli powstanie nowych substancji chemicznych.
Zgodnie z teorią zderzeń szybkość każdego etapu reakcji jest wprost proporcjonalna do:
- liczby zderzeń cząstek biorących udział w danym etapie w jednostce czasu
- stosunku zderzeń efektywnych do całkowitej liczby zderzeń.
Dlaczego nie wszystkie zderzenia są efektywne?
Zderzenia mogą być zbyt łagodne do zaistnienia jakichkolwiek zmian.
Jeżeli cząstki A lub B, albo A i B, mają przed zderzeniem dużą energię
kinetyczną, to może ona być wykorzystana do przezwyciężenia sił odpychania
zbliżających się elektronów. Gdy energia kinetyczna jest dostatecznie duża,
siły odpychania zostają pokonane, a cząsteczki mogą dokonać wymiany
atomów i elektronów tworząc jedną lub więcej nowych cząsteczek.