Druga zasada termodynamiki stwierdza, że w
układzie termodynamicznie izolowanym
istnieje funkcja stanu zwana
entropią
S, której zmiana ΔS w
procesie adiabatycznym
spełnia nierówność  , przy czym równość zachodzi wtedy i tylko wtedy, gdy proces jest odwracalny.
, przy czym równość zachodzi wtedy i tylko wtedy, gdy proces jest odwracalny.
W uproszczeniu można to wyrazić też tak:
- "W
układzie termodynamicznie izolowanym
w dowolnym procesie entropia nigdy nie maleje"
Uwaga!
W wielu opracowaniach pojawia się błąd, polegający na stwierdzeniu, że druga zasada termodynamiki zapewnia formie ciepła istnienie czynnika całkującego. Jest to tylko część treści tej zasady. Najlepiej się o tym przekonać wybierając prosty układ opisany dwoma parametrami. Z matematyki wiadomo, że w takim układzie (dwuwymiarowa przestrzeń stanów), każda forma liniowa ma czynnik całkujący! A zatem tak rozumiana zasada termodynamiki nic by nie wnosiła do takich układów[1].
Definicja w terminach termodynamiki klasycznej
Matematyczny zapis tego faktu to następujące sformułowanie: zmiana
entropii
ΔS w dowolnym
procesie odwracalnym
jest równa całce z przekazu
ciepła
DQ podzielonego przez
temperaturę
T. W
procesie nieodwracalnym
natomiast zmiana entropii jest większa od tej całki. Forma całkowa II zasady termodynamiki wygląda następująco:
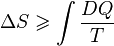
Różnica ta jest miarą nieodwracalności procesu i jest związana z rozpraszaniem energii. Oznaczenie DQ użyte do zapisu przyrostu ciepła ma na celu odróżnienie tego przyrostu od
różniczki
(ozn. dX), ponieważ przyrost ciepła nie jest różniczką żadnej funkcji. Gdyby był różniczką, ciepło byłoby
funkcją stanu
.
Alternatywne sformułowania
Druga zasada termodynamiki może być sformułowana na wiele równoważnych sposobów. Wiele z nich nie wymaga odwoływania się do abstrakcyjnych pojęć, takich jak entropia, umożliwiając łatwiejsze zrozumienie fizycznej istoty tego prawa.
Najszerzej znane alternatywne sformułowania pochodzą od
Clausiusa
:
- "Ciepło nie może samorzutnie przepływać od ciała o temperaturze niższej do ciała o temperaturze wyższej"
oraz od
Lorda Kelvina
:
- "Nie jest możliwy proces, którego jedynym skutkiem byłoby pobranie pewnej ilości ciepła ze zbiornika i zamiana go w równoważną ilość pracy"
Można udowodnić równoważność tych stwierdzeń z powyższym sformułowaniem[2].
Wprowadzając pojęcie
perpetuum mobile
drugiego rodzaju, jako silnik cieplny pobierający energię cieplną z układu i w całości przekształcający ją na pracę, można sformułować drugą zasadę termodynamiki w następujący sposób:
- "Nie istnieje perpetuum mobile drugiego rodzaju"[3]

- Entropia jest
wielkością ekstensywną
, addytywną w danym stanie układu, tj. entropia całego układu jest wówczas sumą entropii wszystkich jego części, będących rozdzielnymi układami makroskopowymi.
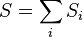
W przypadku połączenia tych części (np. zmieszanie płynów), entropia nie spełnia warunku addytywności.
Wnioski z II zasady Termodynamiki
Silnik cieplny nie może działać bez różnic temperatury
Inne, równoważne, sformułowanie drugiej zasady termodynamiki wiąże się z
silnikiem cieplnym
, czyli urządzeniem zamieniającym ciepło na
pracę
. Zgodnie z tym sformułowaniem, spontaniczny przekaz ciepła może się dokonywać tylko od ciała cieplejszego do zimniejszego. Idealny silnik, pracujący w cyklu przemian odwracalnych, ma
sprawność
η ograniczoną różnicą temperatur ciał, pomiędzy którymi przekazywane jest ciepło:
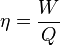
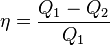
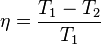
gdzie ciepło jest przekazywane od ciała o temperaturze T1 do ciała o temperaturze T2. Silnik spełniający tę regułę jest nazywany silnikiem
Carnota
.
Z II zasady termodynamiki zastosowanej do silników cieplnych wynika, że nie można ciepła zamieniać na pracę bez ograniczeń, choć jest to zgodne z
I zasadą termodynamiki
. Nie można bez wkładu pracy przesyłać energii termicznej między ciałami mającymi tę samą temperaturę. Oznacza to, że
perpetum mobile
II rodzaju nie istnieje.
Prowadzi to do dalszego wniosku - nie da się w pełni kontrolować procesów statystycznych, np. nie można czerpać energii z przypadkowych ruchów cząstek, takich jak
ruchy Browna
. Z II zasady wynika, że przyrządy do czerpania tego rodzaju energii po pewnym czasie też zaczną się zachowywać przypadkowo, a więc staną się bezużyteczne. Miarą tej przypadkowości jest właśnie temperatura. Aby czerpać energię termiczną z układu, trzeba dysponować czymś zimniejszym niż ten układ.
Śmierć cieplna Wszechświata
Z II zasady termodynamiki wynika też hipoteza tzw. śmierci cieplnej
Wszechświata
. Miałaby ona polegać na tym, iż po jakimś czasie Wszechświat, jako całość, dojdzie do stanu
równowagi termodynamicznej
, czyli będzie miał jednakową temperaturę w każdym punkcie i wymiana energii termicznej całkowicie zaniknie, a co za tym idzie zanikną wszelkie inne rodzaje wymiany energii, które w ten czy inny sposób są zawsze związane ze zmianą temperatury. Teoria śmierci cieplnej jest jednak nadinterpretacją, wynikającą z przeniesienia rozumowania pochodzącego z fizyki fenomenologicznej w dziedzinę przekraczającą zakres jej stosowalności – do
kosmologii
. Taka interpretacja II zasady termodynamiki zakłada bowiem, że Wszechświat jako całość jest
układem izolowanym
, co jest nieprawdą, gdyż rozszerzający się wszechświat jest
układem otwartym
[4].
Paradoks nieodwracalności
Z interpretacją II zasady termodynamiki jest też związany swoisty paradoks. Z jednej strony wynika z niej, że wiele zjawisk, obserwowanych w
skali makroskopowej
może być nieodwracalne. Z drugiej strony termodynamika statystyczna, z której ta zasada się wywodzi, zakłada, że każde jednostkowe zjawisko w
skali mikroskopowej
, czyli w skali pojedynczych
cząstek
jest odwracalne. Mimo że wszystkie zjawiska makroskopowe są sumą odwracalnych zjawisk mikroskopowych, przyjmuje się jednak - wbrew zdrowemu rozsądkowi - możliwość ich nieodwracalności. Paradoks ten przyczynił się do początkowego odrzucenia równania
Boltzmanna
, opisującego procesy nierównowagowe.
Ten paradoks wskazuje na ścisły związek między teorią a pomiarem w fizyce. Interpretacja pomiaru układów wielocząstkowych jest oparta na teoriach tworzonych dla układów makroskopowych. Można powiedzieć, że pomiary te dotyczą sum uśrednionych zjawisk mikroskopowych. Dla takich pomiarów koncepcja entropii jest niezbędna teoretycznie. Gdyby jednak dało się w jakiś sposób przejść do pomiaru tych zjawisk na poziomie pojedynczych cząstek, koncepcja entropii przestałaby być potrzebna. Liczba cząstek w rzeczywistych, makroskopowych układach doświadczalnych jest jednak bardzo duża (rzędu
stałej Avogadra
) i dlatego pomiar większości zjawisk fizycznych na poziomie mikroskopowym jeszcze długo pozostanie poza zasięgiem nauki.
Przypisy
- ↑ "Fizyka statystyczna i termodynamika", R.S Ingarden, A. Jamiołkowski, R. Mrugała, PWN, Warszawa 1990, str. 95-96
- ↑ C.J.Adkins, "Equilibrium thermodynamics", Cambridge University Press,
- ↑ Tablice Fizyczno-Astronomiczne. pod redakcją Witolda Mizierskiego.
Warszawa
:
Adamantan
,
2002
. .
- ↑
http://web.archive.org/web/20061007131456/http://www.ichf.edu.pl/Softmatter/entropia/entropia.pdf
Zobacz też