Liczba masowa (A) to wartość opisująca liczbę
nukleonów
(czyli
protonów
i
neutronów
) w
jądrze
atomu
(
nuklidzie
) danego
izotopu
danego
pierwiastka
. Liczby masowej nie należy mylić z
masą atomową
pierwiastka, która wyznaczana jest metodami chemicznymi, ani też z masą pojedynczego
izotopu
.
Różnice tych wartości wynikają z:
- istnienia
izotopów
,
-
defektu masy
jądra,
- dodatkowego udziału
elektronów
w masie atomowej.
Atomy mające tę samą liczbę masową, ale różną liczbę protonów, nazywa się
izobarami
.
Liczbę masową izotopów pisze się tradycyjnie w górnym, lewym indeksie symbolu pierwiastka. Np. symbol 12C oznacza izotop
węgla
posiadający 12 nukleonów w jądrze - 6 neutronów i 6 protonów, zaś izotop 13C posiada 13 nukleonów - 6 protonów i 7 neutronów. Ogólniejszy zapis ma postać:
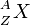
gdzie A - liczba masowa, Z -
liczba atomowa
, X - symbol
pierwiastka
, np.  -
deuter
,
-
deuter
,  -
tryt
,
-
tryt
, 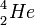 -
hel
-
hel
Zobacz też