 Nie znaleziono szukanej frazy! Poniżej znajduje się fraza najbardziej przypominająca szukaną. Nie znaleziono szukanej frazy! Poniżej znajduje się fraza najbardziej przypominająca szukaną.
Równanie Clapeyrona (stan gazu doskonałego)
Równanie Clapeyrona (stan gazu doskonałego)Równanie Clapeyrona, równanie stanu gazu doskonałego to
równanie stanu
opisujące związek pomiędzy temperaturą, ciśnieniem i objętością
gazu doskonałego
, a w sposób przybliżony opisujący
gazy rzeczywiste
. Sformułowane zostało w 1834 roku przez
Benoîta Clapeyrona
. Prawo to można wyrazić wzorem 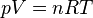
gdzie: Równanie to jest wyprowadzane na podstawie założeń: - gaz składa się z poruszających się cząsteczek;
- cząsteczki zderzają się ze sobą oraz ze ściankami naczynia w którym się znajdują;
- brak oddziaływań międzycząsteczkowych w gazie, z wyjątkiem odpychania w momencie zderzeń cząsteczek;
- objętość (rozmiary) cząsteczek jest pomijana;
- zderzenia cząsteczek są
doskonale sprężyste
;
Równanie to, mimo że wyprowadzone na podstawie założeń, które nigdy nie są spełnione, dobrze opisuje większość substancji
gazowych
w obszarze ciśnień do ok. 100
atmosfer
i temperatury do 300–400 °C, oraz w temperaturze trochę większej od temperatury skraplania gazu. Z równania tego wynika fundamentalny związek między ciśnieniem, temperaturą i liczbą cząstek gazu, z którego wynikają trzy wnioski: - n moli (taka sama liczba cząstek) gazu, przy danej temperaturze i ciśnieniu panującym w naczyniu zajmuje zawsze taką samą objętość, niezależnie od budowy chemicznej tego gazu (V = nRT/p).
- w danej objętości, przy danym ciśnieniu i temperaturze, znajduje się zawsze taka sama liczba moli cząsteczek gazu, niezależnie od jego budowy chemicznej (n = pV/RT)
- n moli gazu zamkniętych w naczyniu o określonej objętości, przy określonej temperaturze, będzie wywierał na jego ścianki zawsze jednakowe ciśnienie, niezależnie od tego, jaki to jest gaz (p = nRT/V).
Określenie równanie Clapeyrona nie jest stosowane powszechnie w odniesieniu do tego wzoru – w literaturze anglojęzycznej równanie to znane jest jedynie jako ideal gas law (prawo gazu doskonałego), podobnie jest w większości innych języków. W
Rosji
równanie to funkcjonuje pod nazwą równania
Mendelejewa
-Clapeyrona.
Równanie Clapeyrona
opisuje przemiany fazowe, m.in. ciecz-gaz. Pod tą nazwą często funkcjonuje też
równanie Clausiusa-Clapeyrona
. Rozszerzeniami równania gazu doskonałego, uwzględniającymi objętość cząsteczek gazu oraz przyciąganie cząsteczek, są
równanie van der Waalsa
oraz
wirialne równanie stanu
. - Przemiany termodynamiczne
Zobacz też-
termodynamika
Linki zewnętrzne
Inne hasła zawierające informacje o "Równanie Clapeyrona (stan gazu doskonałego)":
Nadciśnienie tętnicze
...
Adwentyzm
...
Uznam
...
Fosforan wapnia
...
1972
...
Kwas fosforowy
...
Diakon
...
Aurora
...
Nowa Polityka Ekonomiczna
...
Nowa Anglia
...
Inne lekcje zawierające informacje o "Równanie Clapeyrona (stan gazu doskonałego)":
21 Alkohol i inne używki. Kolizje i wypadki (plansza 1)
...
21 Alkohol i inne używki. Kolizje i wypadki (plansza 2)
...
20 Zachowanie się na drodze wobec pieszych i rowerzystów (plansza 3)
...
|