Reguła Pauliego, zwana też zakazem Pauliego, została zaproponowana przez
Wolfganga Pauliego
w
1925
dla wyjaśnienia zachowania się
fermionów
, czyli cząstek o
spinie
połówkowym. Reguła Pauliego jest szczególnym przypadkiem ogólniejszego
twierdzenia o związku spinu ze statystyką
.
Zakaz Pauliego głosi, że w danym
stanie kwantowym
może znajdować się jeden fermion - albo inaczej, że żadne dwa fermiony nie mogą w jednej chwili występować w dokładnie tym samym stanie kwantowym.
W sformułowaniu szczególnym - Jeżeli wśród
stanów
jednocząstkowych 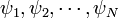 wystąpią choćby dwa jednakowe stany, np. ψ1 = ψ2, to
wyznacznik Slatera
znika tożsamościowo.
wystąpią choćby dwa jednakowe stany, np. ψ1 = ψ2, to
wyznacznik Slatera
znika tożsamościowo.
Zakaz Pauliego w sformułowaniu szczególnym stosuje się ściśle do układu jednakowych
fermionów
które nie oddziałują ze sobą. Dla układu jednakowych
fermionów
, które z sobą oddziałują, ma znaczenie przybliżone.
Zakaz Pauliego odgrywa ważną rolę przy opisie własności
jąder atomowych
i
atomów
. Stanowi punkt wyjścia dla zasady rozbudowy
powłok elektronowych
oraz wyjaśnienia okresowości konfiguracji elektronowych
atomów
.
Reguła ta ma wielkie znaczenie w chemii i fizyce atomowej. Szereg fundamentalnych własności
materii
jest jej wynikiem, gdyż materia jest zbudowana właśnie z fermionów, z których najczęściej spotykane to
protony
,
elektrony
i
neutrony
.
Wynikają stąd implikacje:
- Tworzenie się struktury
orbitalowej
poziomów
elektronów wszystkich atomów, z której z kolei wynikają wszystkie właściwości chemiczne
pierwiastków chemicznych
. Gdyby reguła Pauliego nie obowiązywała dla elektronów, to wszystkie przebywałyby na orbitalu 1s każdego atomu, gdyż elektrony położone na tym orbitalu mają zawsze niższą energię w porównaniu z elektronami zajmującymi wszystkie inne orbitale. W takiej sytuacji wszystkie pierwiastki zachowywałyby się jak
gazy doskonałe
i nie byłoby żadnych przemian chemicznych. Każdy orbital może jednak zostać obsadzony przez co najwyżej dwa elektrony różniące się
spinem
, co stanowi podstawowe prawo mające swe odbicie w
układzie okresowym pierwiastków
.
- Nieprzenikalność materii przez samą siebie. Na skutek działania reguły Pauliego dwa fermiony nie mogą jednocześnie przebywać w tym samym miejscu, jeżeli znajdują się w tym samym stanie kwantowym. W wielu przypadkach uniemożliwia to występowanie pewnych konfiguracji przestrzennych orbitali blisko położonych atomów czy cząsteczek. W związku z tym atomy nie mogą przenikać się nawzajem w dowolny sposób, a w momencie zderzenia dwóch atomów dochodzi albo do ich połączenia w
związek chemiczny
, albo sprężystego odbicia.
- Względna trwałość obiektów materialnych. Z reguły Pauliego wynika, że wszelkie przemiany materii muszą być związane z jakimś efektem energetycznym, gdyż są zawsze związane ze zmianami stanów kwantowych tworzących je fermionów. Każda taka przemiana wymaga przekroczenia pewnej bariery potencjału energetycznego. Przemiany te zawsze podlegają regułom
termodynamiki
.