Stała dysocjacji (obecnie często zwana po prostu stałą jonizacji) to
stała równowagi
reakcji dysocjacji
czyli rozpadu
związków chemicznych
na poszczególne jony, pod wpływem
rozpuszczalnika
, lub pod wpływem np. działania silnego
pola elektrycznego
.
Przykładowo dla
kwasu
HA, ulegającemu reakcji dysocjacji w wodzie:

stała dysocjacji ma postać
![K_{a}=\frac{[H_{3}O^{+}][A^{-}]}{[HA]}](http://upload.wikimedia.org/math/c/d/7/cd7e5b3d5625b84a03d726c13e522e8a.png)
Dla
zasady
B, ulegającej reakcji :
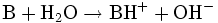
stała dysocjacji ma postać
![K_{b}=\frac{[BH^{+}][OH^{-}]}{[B]}](http://upload.wikimedia.org/math/0/c/4/0c44af20bcadb85a2bd5b087b316d184.png)
W obu przypadkach zostało pominięte stężenie wody, gdyż w warunkach reakcji jest ono prawie stałe i jest wliczone w wartość stałej dysocjacji.
Zamiast stałej dysocjacji można podać wartość
pKa
lub
pKb
, które są miarą mocy odpowiednio kwasu i zasady.
Dla każdego kwasu i zasady można podać tzw. sprzężoną zasadę czy sprzężony kwas (sprzężone pary kwas-zasada), np. dla słabego
kwasu octowego
CH3COOH sprzężoną zasadą jest anion octanowy CH3COO-; dla słabej
zasady amonowej
NH3 (lub w formie uwodnionej NH3·H2O) kwasem sprzężonym jest kation amonowy NH4+.
Dla
wody
(i dla każdego rozpuszczalnika ulegającego
autodysocjacji
) cząsteczki H2O pełnią rolę zarówno kwasu jak i zasady.
Stałe dysocjacji dla sprzężonej pary kwas-zasada spełniają równanie:
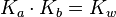 oraz pKa + pKb = pKw
oraz pKa + pKb = pKw
Stała dysocjacji sprzężonego kwasu lub zasady jest jednocześnie równa tzw.
stałej hydrolizy
odpowiedniej soli, np. Ka dla NH4+ jest równe stałej hydrolizy NH4Cl.