Schematyczna reprezentacja procesu mieszania dwóch substancji na drodze dyfuzji
Dyfuzja - proces samorzutnego rozprzestrzeniania się
cząsteczek
lub
energii
w danym ośrodku (np. w
gazie
,
cieczy
lub
ciele stałym
), będący konsekwencją chaotycznych zderzeń cząsteczek dyfundującej substancji między sobą lub z cząsteczkami otaczającego ją ośrodka. Ze względu na skalę zjawiska, rozpatruje się dwa podstawowe rodzaje dyfuzji:
- dyfuzja śledzona (ang. tracer diffusion) to proces mikroskopowy polegający na chaotycznym ruchu pojedynczej ("śledzonej") cząsteczki (przykład:
ruchy Browna
).
- dyfuzja chemiczna to proces makroskopowy obejmujący makroskopowe ilości materii (lub energii), zwykle opisywany równaniem dyfuzji i prowadzący do wyrównywania stężenia (lub temperatury) każdej z dyfundujących substancji w całym układzie.
Podstawowymi prawami opisującymi dyfuzję są
Prawa Ficka
. Pierwsze prawo Ficka stwierdza że:
- strumień cząstek dyfuzji jest proporcjonalny do gradientu stężenia

gdzie:
- J - strumień składnika (masa molowa składnika przepływająca przez jednostkowy przekrój w jednostce czasu)
- D - współczynnik proporcjonalności dyfuzji
- φ -
stężenie
[(ilość substancji) x długość-3],
- x - współrzędna wzdłuż której zachodzi dyfuzja.
Dla chemicznej dyfuzji materii (masy) współczynnik dyfuzji jest nazywany współczynnikiem dyfuzji molekularnej. Dla tej samej substancji, w tych samych warunkach, współczynniki dyfuzji śledzonej i chemicznej są zwykle różne, gdyż drugi z tych współczynników uwzględnia oddziaływania i korelacje pomiędzy trajektoriami poszczególnych dyfundujących cząsteczek.
Dyfuzja zachodzi zarówno w stanie równowagi, jak i poza równowagą termodynamiczną. Dyfuzję śledzoną bada się zwykle w stanie równowagi, a dyfuzję chemiczną w układach nierównowagowych. Dyfuzja w stanie braku równowagi termodynamicznej jest procesem nieodwracalnym, który przybliża stan układu do stanu równowagi termodynamicznej i zwiększa jego
entropię
. Dyfuzja chemiczna zachodząca w stanie równowagi zwana jest samodyfuzją.
Dyfuzja materii jest zjawiskiem aktywowanym termicznie - zwiększenie
temperatury
zwykle prowadzi do zwiększenia tempa dyfuzji. W przypadku większości ciał stałych zależność tę opisuje
równanie Arrheniusa
.
Dyfuzja jest jednym z mechanizmów transportu. W tym kontekście jej bardzo charakterystyczną cechą jest to, że typowa odległość R, o którą przemieszczana jest substancja z obszaru o podwyższonym stężeniu po dostatecznie długim czasie t jest proporcjonalna do
pierwiastka
kwadratowego z
czasu
:
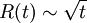
Dla większości substancji powyższa zależność obowiązuje (dla dostatecznie dużych czasów t) nawet wtedy, gdy współczynnik dyfuzji danej substancji zależy od jej stężenia. W pewnych układach obserwuje się jednak procesy, które w obrazie mikroskopowym składają się z szeregu charakterystycznych dla dyfuzji "chaotycznych" zderzeń, w których to jednak procesach obowiązuje zależność

W takich przypadkach mówi się o dyfuzji anomalnej.
Dyfuzja może też dotyczyć
energii
, jej szybkość jest określona przez współczynnik dyfuzji termicznej. Na przykład źródłem
niekonwekcyjnego
transportu ciepła jest wymiana
energii kinetycznej
pomiędzy chaotycznie zderzającymi się
cząsteczkami
, stąd też
równanie przewodnictwa cieplnego
w ciałach stałych jest tożsame równaniu dyfuzji.
W przypadku dyfuzji pędu, o szybkości procesu dyfuzji decyduje współczynnik dyfuzji zwany
lepkością kinematyczną
.
Przykłady dyfuzji
Dyfuzja umożliwia zjawisko
mieszania
się substancji pozostających w fazie
gazowej
lub
ciekłej
. Siłą napędową dyfuzji przy mieszaniu jest dążenie układu do
równowagi termodynamicznej
przez osiągnięcie jak najwyższej
entropii
i jak najniższej
energii swobodnej
. Efektem wolnej, nieskrępowanej dyfuzji w gazach i cieczach jest wyrównywanie się stężeń wszystkich składników w całej objętości
fazy
. Osiągnięcie stanu równowagi nie oznacza jednak zatrzymania dyfuzji. Trwa ona nadal, tyle że dzięki dokładnemu wymieszaniu się wszystkich składników nie prowadzi już do zmian stężenia. Przykładem tego rodzaju dyfuzji jest rozchodzenie się
zapachów
w
powietrzu
.
Jednym z najbardziej znanych przykładów zjawiska fizycznego zdominowanego przez dyfuzję są
ruchy Browna
.
Innym przykładem dyfuzji jest zjawisko
osmozy
, polegające na przemieszczaniu się cząsteczek i jonów przez
błony półprzepuszczalne
, w kierunku wyrównywania się stężenia związku chemicznego lub jonu, zdolnego do przenikania przez błonę. Siła napędową osmozy jest dokładnie to samo, co napędza dyfuzję swobodną w mieszaninach. Różnica polega na tym, że błona przepuszcza tylko wybrane składniki mieszaniny, podczas gdy inne nie.
Odwrócona osmoza
- to przenikanie przez błonę cząsteczek rozpuszczalnika w kierunku odwrotnym niż w osmozie, to znaczy od roztworu o większym stężeniu substancji rozpuszczonej do roztworu o mniejszym stężeniu. Ze względu na to, że osmoza odwrócona zmniejsza entropię układu, musi być ona napędzania np.
napięciem elektrycznym
lub
ciśnieniem
.
W
fizyce ciała stałego
(a więc i w
elektronice
) dyfuzja jest podstawową przyczyną jakiejkolwiek względnej zmiany rozmieszczenia
atomów
w
sieci krystalicznej
zachodzącej pod wpływem
energii termicznej
.
Przykładowe współczynniki dyfuzji[]:
Zobacz też