Kinetyczno-molekularna teoria gazów — mikroskopowy model budowy gazów, umożliwiający makroskopowy opis ich właściwości przy założeniu bardzo dużej ilości
atomów
,
cząsteczek
lub
jonów
.
Założenia teorii
Teoria sformułowana jest przy pewnych założeniach:
- wszystkie ciała składają się z cząstek, których rozmiary można pominąć (epozja)
- cząstki znajdują się w nieprzerwanym, chaotycznym ruchu
- cząstki oddziałują na siebie poprzez
zderzenia sprężyste
, a między zderzeniami poruszają się zgodnie z
zasadami dynamiki Newtona
Założenia te są w przybliżeniu spełnione dla gazów przy niezbyt wysokich
ciśnieniach
w niezbyt niskich temperaturach.
Podstawowe równanie teorii
Podstawowym równaniem teorii kinetycznej gazów jest wzór, który pozwala powiązać parametry poszczególnych cząsteczek z parametrami makroskopowymi gazu, takimi jak:
ciśnienie
,
objętość
,
temperatura
. Ma ono postać

gdzie:
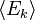 – średnia energia kinetyczna cząsteczki,
– średnia energia kinetyczna cząsteczki,- k –
stała Boltzmanna
,
- i – liczba
stopni swobody
cząsteczki.
Równanie średniej kwadratowej prędkości cząsteczki
Równanie średniej kwadratowej prędkości cząsteczki wynika bezpośrednio z podstawowego równania kinetyczno-molekularnej teorii gazów dla jednego mola gazu doskonałego (cząsteczka ma trzy stopnie swobody):
 ,
,
m jest masą cząsteczki a  średnim kwadratem jej prędkości.
średnim kwadratem jej prędkości.
Stąd

lub, używając masy molowej gazu zamiast masy pojedynczej cząsteczki (Mr = Nam, Na to
stała Avogadra
),

R jest
stałą gazową
.