W zamkniętym naczyniu, w określonej temperaturze T, równowaga reakcji ustaliła się z chwilą osiągnięcia następujących stężeń:

|
[NO2]= 0,12 mol/dm3
|
2NO2 <-> 2NO + O2
|
|
[NO] = 0,48 mol/dm3
|
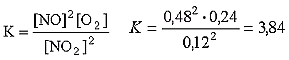
|
|
[O2] = 0,24 mol/dm3
|
ze stechiometrii reakcji mamy:
2 mol NO
2 ------2 mol NO -------------1 mol O
2
x----------------0,48 mol-----------------0,24 mol , czyli przereagowało 0,48 mol NO
2
Ilość moli NO
2 początkowa = ilość moli NO
2 w stanie równowagi + ilość moli, która przereagowała.
C
p NO
2= 0,12 mol/dm
3 + O,48 mol/dm
3 = 0,6 mol/dm
3
Stała równowagi ma wartość K = 3,84. Stężenie początkowe NO
2 wynosiło 0,6 mola/dm
3.