Rozpuszczalność - ilość substancji tworzącej
roztwór nasycony
w określonej ilości (najczęściej w 100 g)
rozpuszczalnika
w określonej
temperaturze
i
ciśnieniu
. Rozpuszczalność określa się w tych samych jednostkach jak
stężenie
, podając dodatkowo warunki, dla jakich została ona ustalona (zwykle są to tzw.
warunki normalne
). Mówiąc inaczej, rozpuszczalność określa, jak dużo danego składnika można rozpuścić w danym rozpuszczalniku w sprecyzowanych warunkach.
Rozpuszczalność nie powinna być mylona z szybkością
rozpuszczania
. Rozpuszczalność jest pojęciem
termodynamicznym
(tzn. opisuje
stan równowagi
), a rozpuszczanie dotyczy
kinetyki
(tzn. opisuje szybkość procesu). Substancje o wysokiej rozpuszczalności niekoniecznie rozpuszczają się szybko.
W pewnych warunkach może dochodzić do przekroczenia rozpuszczalności danej substancji, prowadząc do powstawania
metastabilnych
roztworów przesyconych
.
Rozpuszczalnik może być cieczą lub ciałem stałym, a substancja rozpuszczona gazem, cieczą, lub ciałem stałym.
Wpływ warunków
Rozpuszczalność
substancji
zależy od:
Pojęcie rozpuszczalności odnosi się zwykle do specyficznej
fazy
. Tak wiec
aragonit
i
kalcyt
mają generalnie różną rozpuszczalność, chociaż chemicznie są tą samą substancją (węglan wapnia).
Rozpuszczalniki
polarne
(np. woda) mają tendencje do lepszego rozpuszczania substancji polarnych lub jonowych (
hydrofilowych
, zaś niepolarne (np.
tłuszcz
lub
toluen
) rozpuszczają lepiej substancje niepolarne (
lipofilowe
). Często podawane jest to jako reguła "podobne rozpuszcza podobne". Jest to czasem podstawą klasyfikacji substancji (np. podział
witamin
na rozpuszczalne w wodzie i rozpuszczalne w tłuszczach). Reguła ta jest też podstawą mechanizmu działania
detergentów
.
Ze wzrostem temperatury, rozpuszczalność najczęściej rośnie dla
cieczy
i
ciał stałych
, zaś maleje dla
gazów
ale znanych jest wiele wyjątków od tej reguły (np. rozpuszczalność
siarczanu wapnia
w wodzie maleje ze wzrostem temperatury)
Efekt ciśnienia na rozpuszczalność faz skondensowanych (ciecze, ciała stałe) jest stosunkowo niewielki i przeważnie ignorowany w praktyce.
Rząd wielkości
Różne substancje mogą się znacznie różnić rozpuszczalnością. Substancje czasem określane są terminami "nierozpuszczalna", "słabo rozpuszczalna", "dobrze rozpuszczalna", itd. Jednakże takie klasyfikacje mają ograniczoną użyteczność. Na przykład rozpuszczalność 1 g/kg może być uważana w niektórych zastosowaniach za "słabą" (np. w
inżynierii procesowej
), a w innych za "wysoką" (np. przy opisie procesu korozji lub w chemii środowiska naturalnego). Substancje zupełnie nierozpuszczalne (jeśli w ogóle istnieją) są rzadkie. Współcześnie chemia często zajmuje się rozpuszczalnościami o
rzędzie wielkości
od 10-12 kg/kg (
ppt
) do zupełnej mieszalności z rozpuszczalnikiem.
Gazy
Dla gazów
prawo Henry'ego
mówi, że rozpuszczalność gazów w cieczach jest proporcjonalna do
ciśnienia parcjalnego
tego gazu:
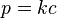
gdzie: p –
ciśnienie parcjalne
gazu (atm), k – stała zależąca od temperatury, rozpuszczalnika i gazu (na przykład dla
tlenu
w wodzie w temperaturze 25 °C stała k wynosi 769,2 l•atm/mol ), c – stężenie gazu rozpuszczonego w cieczy (mol/l).
Pojęcia rozpuszczalności zwykle nie stosuje się do gazowych rozpuszczalników. Zamiast rozpuszczalności w gazach mówi się zwykle o
prężności pary
nad fazą ciekłą lub stałą.
Roztwory stałe
Oprócz roztworów ciekłych, znane są też roztwory stałe, tzn. takie, gdzie roztwór jest ciałem stałym. Układy takie maja duże znaczenie praktyczne, gdyż substancje rozpuszczone mogą silnie zmieniać własności fizyczne i chemiczne roztworu stałego. Przykładem tego są silnie zróżnicowane właściwości
stopów
żelaza
(zob.
stop żelaza z węglem
) i
aluminium
w zależności od zawartości różnych składników. Roztworami stałymi jest też wiele
minerałów
.
Zobacz też
Linki zewnętrzne