|
|
Aktualna kategoria:
Nauka » Chemia » Liceum - lekcje
| 1 | | | ... | | | 4 | | | 5 | | | 6 | | | 7 | | | 8 | | | 9 | | | 10 | | | 11 | | | 12 | | | 13 | | | 14 | | | 15 | | | 16 | | | 17 | | | 18 | | | 19 | | | 20 | | | 21 | | | 22 | |
|
Lekcja: "Elementy termodynamiki część 2"
|
|
|
|
Wyznacz entalpię reakcji: CaO(s) + CO 2(g) → CaCO 3(s)
mając dane:
ΔH0CaO(s) = ΔH01 = -636kJ
ΔH0CO2(g) = ΔH02 = -394kJ
ΔH0CaCO3(s) = ΔH03 = -1210kJ
CaO(s) → Ca(s) + 1/2 O2(g) ΔH01 = -636kJ/mol
CO2(g) → C(s) + 1/2 O2(g) ΔH01 = -394kJ/mol
Ca(s) + C(s) + 3/2 O2(g) → CaCO3(s) ΔH03 = -1210kJ/mol
|
Molowe entalpie standardowe pierwiastków są równe zeru.
|
Układamy cykl termochemiczny
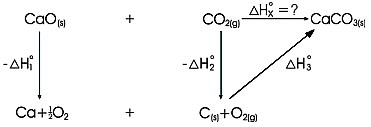
|
|
|
|
|
Pobierz lekcję
|
Udostępnij link do tej lekcji innym uczniom:
|
|