Absorpcja – w
optyce
proces pochłaniania
energii
fali elektromagnetycznej
przez
substancję
. Natężenie
światła
wiązki przechodzącej przez substancję ulega zmniejszeniu nie tylko w wyniku absorpcji, lecz również na skutek
rozpraszania światła
. O ile jednak promieniowanie rozproszone opuszcza ciało, to część zaabsorbowana zanika powodując wzrost energii wewnętrznej tego ciała.
Mechanizm absorpcji
W procesie absorpcji
światło
zachowuje się jak strumień
cząstek elementarnych
i może być pochłaniane tylko w określonych porcjach, których wielkość zależy od
częstotliwości
światła ν
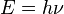
gdzie h –
stała Plancka
.
Kwant
światła, czyli
foton
niosący tę określoną porcję energii może oddziaływać z
elektronem walencyjnym
w
atomie
substancji ośrodka. Jeżeli energia fotonu równa jest różnicy energii pomiędzy dowolnym
stanem wzbudzonym
elektronu
a
stanem podstawowym
, wówczas foton zostanie pochłonięty (następuje absorpcja fotonu). Gdy energia fotonu jest inna, wówczas albo przechodzi on przez substancję bez przeszkód, albo jest rozpraszany. Na skutek absorpcji fotonu atom przechodzi w stan wzbudzenia o wyższej energii. Wzbudzone atomy powracają do stanu podstawowego emitując foton o takiej samej lub mniejszej energii. Zmniejszenie energii emitowanego fotonu w porównaniu z energią fotonu absorbowanego nosi nazwę
luminescencji
. Układ
poziomów energetycznych
elektronów w atomach, czas życia stanów wzbudzonych i sam proces absorpcji wynika z praw
mechaniki kwantowej
.
Absorpcja w gazach atomowych
W zimnych gazach atomowych poziomy energetyczne charakteryzujące stany wzbudzenia leżą stosunkowo daleko od siebie. Dlatego substancje te mogą absorbować tylko niektóre fotony o ściśle określonych energiach (i częstotliwościach). Jeżeli widmo światła padającego jest widmem ciągłym, powoduje to powstawanie w tym widmie ciemnych linii. Po raz pierwszy zjawisko absorpcji zostało zaobserwowane w widmie słonecznym przez
Fraunhofera
[1] a jego prawidłową interpretację podał
Bunsen
i
Kirchhoff
[2].
Możliwa jest również absorpcja przez wzbudzony atom (
absorpcja ze stanów wzbudzonych
).
Absorpcja w gazach cząsteczkowych
W przypadku cząsteczek układ poziomów energetycznych elektronów jest dużo bardziej złożony, ponieważ oprócz poziomów związanych z konfiguracją elektronów dochodzą jeszcze poziomy oscylacyjne – związane z drganiami atomów wewnątrz cząsteczki i poziomy rotacyjne – związane z obrotami całej cząsteczki. Poziomy energetyczne leżą tak blisko siebie, że zlewają się w całe pasma o różnej szerokości.
Wykorzystanie zjawiska absorpcji
W wyniku absorpcji światła przechodzącego przez
substancje
(np.
gaz
) z
widma światła
padającego zostają usunięte fotony o określonej częstotliwości. Na tej podstawie można stwierdzić, przez jakie substancje przechodziło światło. Zjawisko to wykorzystuje się do badania składu chemicznego
mieszanin
związków chemicznych
, gazów otaczających
gwiazdy
, obłoków gazowych we
Wszechświecie
. Zajmuje się tym
spektroskopia
absorpcyjna.
Wielkości charakteryzujące absorpcję światła
Ilościową miarą wielkości absorpcji są
transmitancja
i
absorbancja
promieniowania
.
Zdolność absorpcyjna
Ułamek światła pochłoniętego.
Absorbancja
Wielkość absorpcji światła można obliczyć na podstawie
prawa Bouguera
. Zgodnie z tym prawem natężenie światła zmienia się wykładniczo wraz z grubością substancji. Aby ułatwić obliczanie wielkości absorpcji, wprowadzono w miejsce natężenia wielkość addytywną – absorbancję zwaną również gęstością optyczną. Oznacza się ją symbolem ABS lub A.
Absorbancja jest miarą absorpcji promieniowania i wyraża się wzorem

gdzie
- Io – natężenie światła padającego,
- I – natężenie światła po przejściu przez absorbujący ośrodek.

Absorbancję naturalną wyrażoną wzorem

nazywa się również ekstynkcją promieniowania elektromagnetycznego.
Transmitancja
Transmitancja wskazuje, jaka część promieniowania padającego została przepuszczona przez substancję. Wyraża się ona wzorem
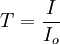
Można ją również wyrażać w procentach
![T \left[ \% \right] =\frac{I}{I_{o}}\cdot 100%](http://upload.wikimedia.org/math/0/b/4/0b4c56a4951d5989a415093ddd17895c.png)
Absorbancja powiązana jest z transmitancją wzorem

Przypisy
- ↑ J. Fraunhofer, Gilbert's Ann. 56, 1817.
- ↑ Robert Bunsen, Gustaw Kirchhoff, Untersuchungen und die Spektren der chemischen Elemente, Abh, kgl.Akad. Wiss. Berlin, 1861, 1863.