|
izotop
Izotopy
Izotopy - to atomy, które posiadają ściśle określoną liczbę protonów (liczba atomowa) oraz neutronów.
Różne nuklidy tego samego pierwiastka są jego izotopami.
Atomy danego izotopu charakteryzują się więc taką samą liczbą atomową (Z) i liczbą masową (A).
A = N + Z
A – liczba masowa
Z – liczba atomowa
N – liczba neutronów w danym jądrze
Niewielkie różnice własności fizykochemicznych izotopów tego samego
pierwiastka, wynikające z różnej masy lub geometrii jąder atomowych, nazywamy
efektem izotopowym. Różnice te są tym większe, im większy jest rozrzut ich mas względem siebie. Różnice w
masach atomowych izotopów powodują, że w formie czystej mają one inną gęstość,
temperaturę wrzenia, topnienia i sublimacji. Różnice te rozciągają się także na
związki chemiczne o różnym składzie izotopowym. Różnica mas izotopów powoduje też występowanie niewielkich różnic w ich reaktywności.
Nie ma ona wpływu na kierunek reakcji chemicznych, w których one uczestniczą, ale wpływa na szybkość tych reakcji.
Ze względu na trwałość izotopy dzielimy na:
W naturze większość pierwiastków chemicznych występuje jako mieszanina wielu swoich izotopów, przy czym proporcje pomiędzy nimi są z dużą
dokładnością stałe. Procentowy udział danego izotopu nosi miano
względnej częstości występowania izotopu. Zjawisko izotopii powoduje, że
masy atomowe pierwiastków nie są liczbami całkowitymi.
Przykłady izotopów
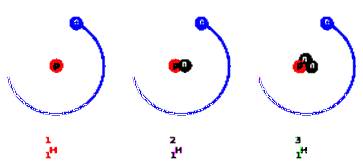
Izotopy wodoru (Z = 1)
- 1H – prot - Z = 1; A = Z = 1; N = 0
- 2H – deuter - Z = 1; A = 1 + 1 = 2; N = 1
- 3H – tryt - Z = 1; A = 1 + 2 = 3; N = 2
Izotopy tlenu
- 168O - Z = 8; A = 8 + 8 = 16; N = 8
- 178O - Z = 8; A = 8 + 9 = 17; N = 9
- 188O - Z = 8; A = 8 + 10 = 18; N = 10
Inne hasła zawierające informacje o "izotop":
Płyn Lugola
po
wybuchu w elektrowni atomowej w Czarnobylu
w celu zapobieżenia wchłanianiu
radioaktywnego
izotopu
jodu
131I z opadów promieniotwórczych powstałych w wyniku wybuchu i pożaru ...
Lantan
cieplna
13,5
W/(m*K)
Potencjały jonizacyjne
I. 538,1 kJ/molII. 1067 kJ/molIII. 1850,3 kJ/molIV. 4819 kJ/molNajbardziej stabilne izotopy
izotop
wyst.
o.p.r.
s.r.
e.r.
MeV
p.r.
137La
{syn.}
6×104
lat
w.e.
0,600137
Ba
138La0,09%1,05×1011
lat
w.e.
β-
1,7371,044138
Ba
138
Ce
139La99,91%stabilny izotop z 82
neutronami
140La
{syn.}
40,28
godzin
β-
3,761140
Ce
Jeżeli nie podano inaczej, ...
Cez
J/(kg*K)
Konduktywność
4,89×106
S
/m
Przewodność cieplna
35,9
W/(m*K)
Potencjały jonizacyjne
I. 375,7 kJ/molII. 2234,3 kJ/molIII. 3400 kJ/molNajbardziej stabilne izotopy
izotop
wyst.
o.p.r.
s.r.
e.r.
MeV
p.r.
133Cs100%stabilny izotop z 78
neutronami
134Cs
{syn.}
2,0648
lat
w.e.
β-
1,2292,059134
Xe
134
Ba
135Cs
{syn.}
2,3×106
lat
β-
0,269135
Ba
137Cs
{syn.}
30,07
lat
β-
1,176137
Ba
Jeżeli ...
Ruten
J/(kg*K)
Konduktywność
13,7×106
S
/m
Przewodność cieplna
117
W/(m*K)
Potencjały jonizacyjne
I. 710,2 kJ/molII. 1620 kJ/molIII. 2747 kJ/molNajbardziej stabilne izotopy
izotop
wyst.
o.p.r.
s.r.
e.r.
MeV
p.r.
96Ru5,52%stabilny izotop z 52
neutronami
98Ru1,88%stabilny izotop z 54
neutronami
99Ru12,7%stabilny izotop z ...
Technet
J/(kg*K)
Konduktywność
6,7×106
S
/m
Przewodność cieplna
50,6
W/(m*K)
Potencjały jonizacyjne
I. 702 kJ/molII. 1470 kJ/molIII. 2618 kJ/molNajbardziej stabilne izotopy
izotop
wyst.
o.p.r.
s.r.
e.r.
MeV
p.r.
97Tc
{syn.}
2,6×106
lat
w.e.
0,32097
Mo
97mTc
{syn.}
90
dni
i.t.
97Tc98Tc
{syn.}
4,2×106
lat
β-
1,35798
Ru
99Tc
{syn.}
2,11×105
lat
β-
3,03499
Ru
99mTc
{syn.}
6,01
h
i.t.
0,14399TcJeżeli nie podano inaczej, dane dotyczą
warunków ...
Niob
kJ/molIII. 2416 kJ/molIV. 3700 kJ/molV. 4877 kJ/molVI. 9847 kJ/molVII. 12100 kJ/molNajbardziej stabilne izotopy
izotop
wyst.
o.p.r.
s.r.
e.r.
MeV
p.r.
91Nb
{syn.}
680
lat
w.e.
1,23591
Zr
92Nb
{syn.}
3,47×107
lat
w.e.
β-
2,0060,35692
Zr
92
Mo
93Nb100%stabilny izotop z 52
neutronami
93mNb
{syn.}
16,13
lat
i.t.
0,03193Nb94Nb
{syn.}
2,03×104
lat
β-
0,47194
Mo
Jeżeli nie podano ...
Cyrkon (pierwiastek)
kJ/molII. 1270 kJ/molIII. 2218 kJ/molIV. 3313 kJ/molV. 7752 kJ/molVI. 9500 kJ/molNajbardziej stabilne izotopy
izotop
wyst.
o.p.r.
s.r.
e.r.
MeV
p.r.
88Zr
{syn.}
83,4
dni
w.e.
88
Y
89Zr
{syn.}
78,4
h
w.e.
β+
0,90289
Y
89Y90Zr51,45%stabilny izotop z 50
neutronami
91Zr11,22%stabilny izotop z 51
neutronami
92Zr17,15%stabilny ...
Itr
kJ/molIV. 5847 kJ/molV. 7430 kJ/molVI. 8970 kJ/molVII. 11190 kJ/molVIII. 12450 kJ/molNajbardziej stabilne izotopy
izotop
wyst.
o.p.r.
s.r.
e.r.
MeV
p.r.
87Y
{syn.}
3,35
dni
w.e.
87
Sr
88Y
{syn.}
106,6
dni
β+
88
Sr
89Y100%stabilny izotop z 50
neutronami
90Y
{syn.}
2,67
dni
β-
2,2890
Zr
91Y
{syn.}
58,5
dni
β-
1,5491
Zr
Jeżeli nie podano ...
Tytan (pierwiastek)
kJ/molIV. 4174,6 kJ/molV. 9581 kJ/molVI. 11533 kJ/molVII. 13590 kJ/molVIII. 16440 kJ/molNajbardziej stabilne izotopy
izotop
wyst.
o.p.r.
s.r.
e.r.
MeV
p.r.
44Ti
{syn.}
63
lata
w.e.
0,26844
Sc
46Ti8,0%stabilny izotop z 24
neutronami
47Ti7,3%stabilny izotop z 25
neutronami
48Ti73,8%stabilny izotop ...
Skand
kJ/molIV. 7090,6 kJ/molV. 8843 kJ/molVI. 10679 kJ/molVII. 13310 kJ/molVIII. 15250 kJ/molNajbardziej stabilne izotopy
izotop
wyst.
o.p.r.
s.r.
e.r.
MeV
p.r.
45Sc100%stabilny izotop z 24
neutronami
46Sc
{syn.}
83,79
dni
β-
2,36746
Ti
47Sc
{syn.}
3,349
dni
β-
0,60047
Ti
48Sc
{syn.}
43,7
dni
β-
3,99448
Ti
Jeżeli nie podano inaczej, ...
Inne lekcje zawierające informacje o "izotop":
Układ okresowy pierwiastków (plansza 6)
(liczbę atomową) od liczby masowej (w tym przypadku 64).
Liczba neutronów w izotopie 64Ni wynosi 36.
...
Stechiometria wzorów i równań chemicznych (plansza 4)
jednostki masy unit (u).
Wzorcem dla określenia unitu stał się w 1961 roku izotop węgla 12C.
Za atomową jednostkę masy (u) przyjęto 1/12 masy izotopu węgla ...
217 Nauka i technika (plansza 3)
(włoski fizyk), który bombardując neutronami atomy niektórych pierwiastków, otrzymał pierwszy sztuczny radioaktywny izotop uranu. Odkrycia i badania nad właściwościami oraz budową jądra atomu przyniosły ...
|