|
Polon
Polon| Polon | | 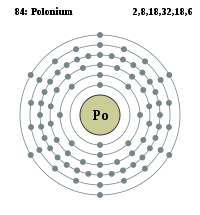 | Rozmieszczenie elektronów na powłokach w atomie polonu |
Rozmieszczenie elektronów na powłokach w atomie polonu | | Dane ogólne | | Nazwa, symbol,
l.a.
| Polon, Po, 84 | | Grupa, okres, blok |
16 (VIA)
, 6,
p
| | Właściwości metaliczne |
półmetal
| | | | | Najbardziej stabilne izotopy |
|---|
|
| Jeżeli nie podano inaczej, dane dotyczą
warunków normalnych (0 °C, 1013,25 hPa)
|
Polon (Po,
łac.
polonium) –
pierwiastek chemiczny
z grupy
metaloidów
bloku p
w
układzie okresowym
. Nazwa pochodzi od
łacińskiej
nazwy
Polski
. Historia odkryciaPierwiastek ten został odkryty w
1898
r. przez
Marię Skłodowską-Curie
i
Piotra Curie
– w tym samym roku co
rad
. Curie nadała mu nazwę na cześć Polski, która była wówczas pod zaborami, licząc na to, iż odkrycie nagłośni ten fakt na arenie międzynarodowej. Został on w ten sposób prawdopodobnie pierwszym pierwiastkiem, którego nazwa nosi w sobie wątek polityczny[1]. Właściwości radioaktywnePolon właściwy jest silnie
radioaktywnym
, srebrzystoszarym
metalem
. Jego własności fizyczne i chemiczne zbliżone są do
selenu
. Polon jest silnym emiterem
promieniowania alfa
– miligram polonu-210 emituje tyle samo cząstek alfa, co 4,5 grama radu-226. Próbka polonu emanuje niebieską poświatą – jest to efekt
wzbudzenia
otaczającego ją powietrza. Jeden gram polonu wydziela 140
watów
mocy, ogrzewając się przy tym do ponad 500 °C[2]. Z tego względu był on niegdyś używany jako lekkie źródło ciepła w satelitach i pojazdach kosmicznych, np. w radzieckich
Łunochodach
do ogrzewania podzespołów podczas zimnych nocy księżycowych. Obecnie jest jeszcze czasami stosowany jako wygodne, wysokowydajne źródło
cząstek alfa
. IzotopyPosiada 33
izotopy
z przedziału mas 188-220. Nie posiada trwałych izotopów. Względnie najtrwalszy jest izotop 209 (okres połowicznego rozpadu 103 lata), paradoksalnie nie występuje on jednak naturalnie, lecz został otrzymany w wyniku sztucznej syntezy jądrowej poprzez bombardowanie
bizmutu
neutronami
. Najtrwalszym, naturalnie występującym izotopem jest izotop 210.
Okres połowicznego rozpadu
tego izotopu to 138,3 dni. Produktem tego rozpadu jest stabilny izotop ołowiu 206Pb. WystępowaniePolon występuje w skorupie ziemskiej w śladowych ilościach w rudach
uranu
oraz jako
tlenek
. Jego stężenie w tych rudach jest jednak tak małe, że przemysłowo opłaca się go otrzymywać na drodze wcześniej wspomnianego bombardowania bizmutu neutronami: 
Jego światowa produkcja wynosi ok. 100 gramów rocznie[2]. Ilość polonu w skorupie ziemskiej jest na tyle mała, że nie podaje się żadnych, nawet szacunkowych danych na ten temat. Związki chemiczneZnanych jest kilkanaście związków chemicznych polonu: tlenki PoO2 i PoO3, wodorek PoH2, wodorotlenek Po(OH)2, halogenki, np. PoCl2, PoBr4, siarczek PoS i
związki metaloorganiczne
. Związki te nie mają jednak żadnego praktycznego zastosowania ze względu na gigantyczny koszt produkcji samego polonu. PoF6 był używany w latach 60. XX w., w
ZSRR
jako aktywator lakierów luminescencyjnych stosowanych w
lampach
, obecnie został już jednak zastąpiony tańszymi zamiennikami. Działanie na organizmy żywePolon wprowadzony do organizmu jest silnie toksyczny.
LD50
dla polonu wynosi ok. 1
mikrograma
, co czyni go ok. 250 000 razy bardziej trującym niż
cyjanowodór
. Emitowane cząstki alfa z łatwością niszczą strukturę tkanek ludzkiego organizmu, jeśli tylko dostanie się on tam poprzez inhalację, połknięcie lub absorpcję. Polon nie przenika przez skórę, toteż znajdując się na zewnątrz ciała nie stanowi tak wielkiego zagrożenia. Izotopy polonu 214Po i 218Po, jako produkty rozpadu
radonu
w śladowych ilościach znajdują się w powietrzu wewnątrz pomieszczeń. Dodatkowe zagrożenie stwarza
palenie tytoniu
, do którego liści przenika polon obecny w
nawozach fosforowych
. Duże stężenie polonu-210 stwierdzono w organizmie
Aleksandra Litwinienki
, otrutego w listopadzie
2006
roku w Londynie. Polon prawdopodobnie pochodził z jednego z rosyjskich reaktorów jądrowych i został mu podany w herbacie. Litwinienko zmarł w ciągu 23 dni. PrzypisyPublikacja jest udostępniona w encyklopedii serwisu Szkolnictwo.pl. Treść objęta jest licencją GNU Wolnej Dokumentacji w wersji 1.1 lub dowolnej pózniejszej opublikowanej przez Free Software Foundation i została ona opracowana na podstawie Wikipedii, tutaj możesz znaleźć artykuł źródłowy oraz autorów.
Inne hasła zawierające informacje o "Polon":
Lantan
...
Cez
...
Ruten
...
Technet
...
Niob
...
Cyrkon (pierwiastek)
...
Itr
...
Tytan (pierwiastek)
...
Skand
...
Neon (pierwiastek)
...
Inne lekcje zawierające informacje o "Polon":
Układ okresowy pierwiastków (plansza 22)
grupy tlenowców należą: tlen (O), siarka (S), selen (Se), tellur (Te) oraz Polon (Po).
Wszystkie występują w przyrodzie w stanie wolnym i w związkach, w ...
Pierwiastki bloku p (plansza 22)
tlenu OF2).
Wraz ze wzrostem masy atomowej słabnie ich charakter niemetaliczny.
Selen jest fotoprzewodnikiem a Polon metalem.
...
139. Przemiany w kulturze i życiu codziennym (plansza 8)
dziedzinie mikrobiologii, małżonkowie Piotr Curie i Maria Skłodowska-Curie (odkryli pierwiastki rad i Polon) wraz z Henrim Becquerelem uczynili wielkie osiągnięcia w dziedzinie badań nad ...
|